有機化合物の反応にオゾン分解という反応があります。
オゾン分解は教科書に掲載されていないにもかかわらず結構頻出。
どれくらいかというと毎年3~4大学程度で出題されているくらい。
なんでこんなに出やすいかというと
- 大学の化学の授業で必ず扱われる反応である。(大学で化学の授業をしている先生が入試問題を作るときに、題材として思いつきやすい)
- 原理はともかくとして、反応の結果はシンプルなのでリード文をつければ高校生でも理解できる(その場で読解力・思考力を問う問題として出題しやすい)
- 炭素間二重結合からケトンをつくる反応であるので、シストランス異性体やカルボン酸の反応をまとめて問うことができる。
から。
あまりにも有名すぎて、教科書に載ってないにもかかわらず説明なしで出題されることも少なからずあるので、できれば覚えておきたいところ。
ただ現実問題大学で習う反応なので、難しい専門用語を多用して高校生が大学受験用に勉強するにはわかりやすく書かれていないのが現状。
そこでこの記事では細かい原理や反応機構はバッサリ省略して大学入試に特化してオゾン分解を説明します。
オゾン分解ってどんな反応?
その名の通り、オゾンを使って有機化合物を分解する反応で、炭素-炭素間の二重結合を切断してケトン2分子をつくります。
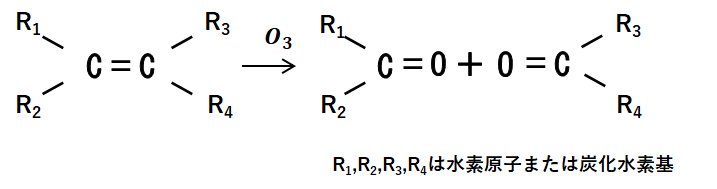
反応結果としては炭素-炭素間の二重結合をちぎってそこに酸素をくっつけるだけなのでわかりやすいですね。
できる化合物は図のRが水素原子なのか炭化水素基なのかによってかわり、両方炭化水素基ならケトン、片方が水素でもう片方が炭化水素基ならアルデヒド、両方が水素原子ならアルムアルデヒドになります。
例)
以下の物質にオゾンを作用させてると、オゾン分解されてホルムアルデヒドとアセトアルデヒドになります。
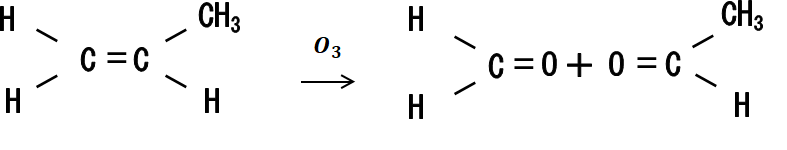
入試問題では未知の化合物をオゾン分解して2つの未知化合物を作り出し、さらにその2つの有機化合物の構造を実験で求め、最後にオゾン分解する前の有機化合物の構造を答えさせるような問題が頻出です。
例題
ある有機化合物X1molにオゾンを作用させると、有機化合物AとBがそれぞれ1mol生じた。Aはクメン法でベンゼンからフェノールを製造するときの副生成物としても得られる。
また、Bはエタノールを酸化したときに得られる化合物である。
Xの構造式を記せ。
解答
オゾンを作用させると書いてあるので、オゾン分解しているんですね。
オゾン分解の結果有機化合物A,Bがそれぞれ1molできているので、ひとつの炭素-炭素間二重結合が切断されていそうですね。
後続の文章からA,Bの構造を決定し、オゾン分解の逆の操作をすればXがわかりそうです。
まずAですが、クメン法の副生成物でオゾン分解でできるとあることから、アセトンであることがわかりますね。
次にBですが、エタノールを酸化して得られるということから、アセトアルデヒドであることがわかります。
エタノールの酸化ということで酢酸も当てはまりそうですが、オゾン分解ではカルボン酸は発生しえません。(カルボン酸だとすると、オゾン分解の前の化合物が炭素-炭素間二重結合にヒドロキシ基が存在することになりますが、こんな構造が不安定だからです。)
A,Bの構造式がわかったのでオゾン分解の逆の操作、炭素-酸素二重結合をちぎってふたつくっつけるとXがわかりますね。

オゾン分解の入試問題
オゾン分解は難易度の高い大学でたびたび扱われるため一度入試問題で経験しておくべきです。
近年の入試問題での出題例をあげておきます。
なお、大学によっては説明なしで出題されることもあります。
2020年 前期神戸大 Ⅲ
2020年 前期名古屋大 問題Ⅳ
2021年 前期九州大 〔4〕
まとめ
大学入試向けオゾン分解の解説でした。
オゾン分解は教科書には載っていないものの比較的出題頻度が高いので、リード文なしでも解けるようにしておけばかなりやりやすくなります!
【関連記事】


コメント
O3の余ったOはどうなりますか?余った同士でO2になるとかO3になるとか、どうなるのか知りたいです