酸化剤・還元剤のはたらきから酸化還元反応の反応式のつくりかたを解説します。
酸化剤の種類と変化

還元剤の種類と変化

酸化還元反応式のつくりかた
酸化還元反応式は酸化剤の水溶液中での変化と還元剤の水溶液中での変化をもとにしてつくることができます。
- 酸化剤・還元剤の水溶液中での変化から半反応式をつくる
- 酸化剤・還元剤の半反応式から電子e-を消去してひとつの反応式をつくる
- 半反応式中で省略されているイオンをおぎなって完成させる
という順番で作っていきます。
半反応式のつくりかた
半反応式は以下のような手順でつくります。
- 反応前後で酸素の数がそろうように酸素を加える
- 反応前後で水素の数がそろうように水素イオンを加える
- 反応前後で電子の数がそろうように電子を加える
例 二酸化硫黄と硫化水素の酸化還元反応式をつくる
例ととして二酸化硫黄と硫化水素の酸化還元反応の反応式をつくってみます。
二酸化硫黄の半反応式をつくる
以下のように、二酸化硫黄が還元によって硫黄になる変化から、
酸素の数をあわせるために水を加える、水素の数をあわせるために水素イオンを加える
イオンの価数をあわせるために電子を加えるという順番で数をあわせた半反応式をつくります。
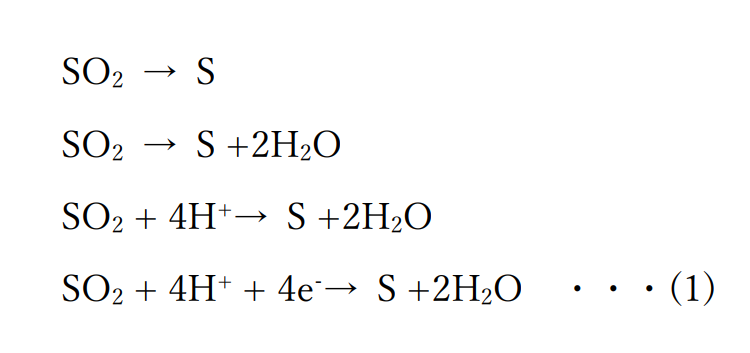
硫化水素の半反応式をつくる
以下のように、硫化水素が酸化によって硫黄になる変化から、
この場合は酸素が登場しないので水を加える必要はなく、水素の数をあわせるために水素イオンを加える、イオンの価数を合わせるために電子を加えるという順番で数をあわせた反応式をつくります。
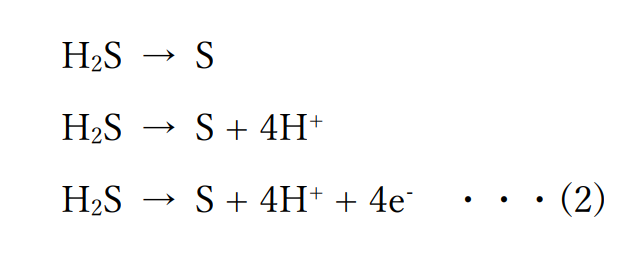
半反応式から電子を消去してひとつの半反応式をつくる
酸化剤と還元剤の半反応式2つから電子を消去してひとつの反応式をつくります。
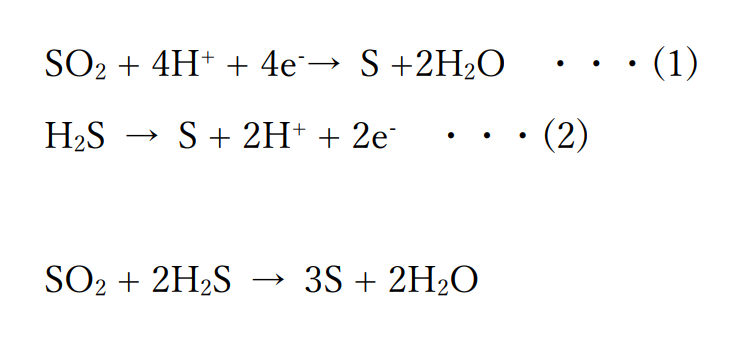
(1)+(2)×2をおこなうことによって電子を消去した酸化還元反応式ができます。
今回の式では省略されたイオンは存在しないためこれで酸化還元反応式が完成です。
例題
過マンガン酸カリウムの硫酸酸性水溶液と過酸化水素の酸化還元反応の化学反応式を記せ。
例題の解答
過マンガン酸カリウムの水溶液中での変化から、酸素、水素イオン、電子の順に数をあわせると以下のようになります。
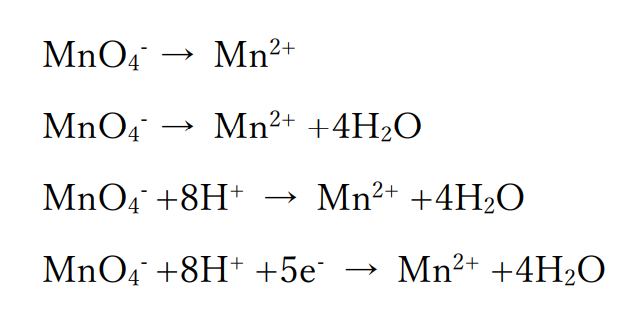
また、過酸化水素の水溶液中での変化から、酸素がすでにそろっているので水素イオン、電子の順にあわせると以下のようになります。
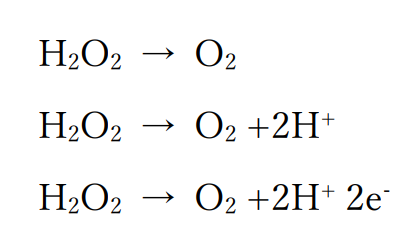
これら2式から電子を消去するように足し合わせると、
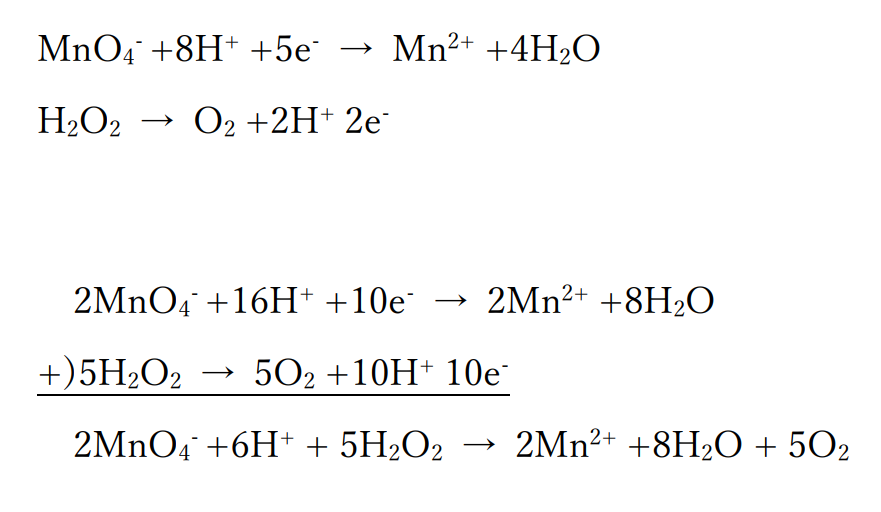
ここからイオンがでてこないように省略されているカリウムイオン、硫酸イオンを補うと、過マンガン酸カリウムと過酸化水素の化学反応式がえられます。
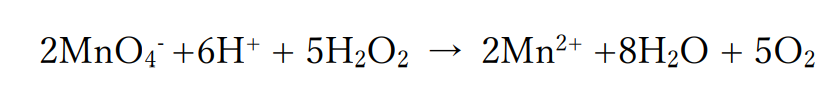
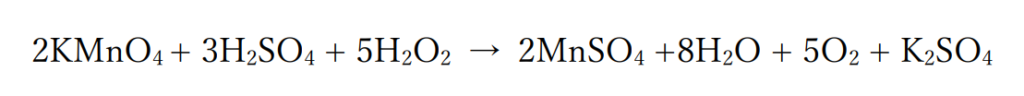


コメント