硝酸を工業的に生産する方法はオストワルト法とよばれています。
オストワルト法ではアンモニアと酸素を原料として三段階で製造します。
オストワルト法
アンモニアを酸化する
アンモニアと酸素を反応させて、一酸化窒素を得ます。
この反応は起こりにくいので、触媒として白金を用いて高温で行います。
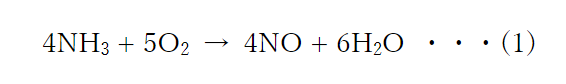
一酸化窒素は二酸化窒素になる
一酸化窒素は酸化されやすい物質で、空気中で自然に二酸化窒素になります。
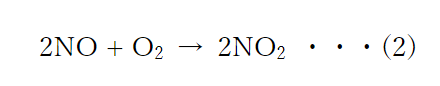
二酸化窒素を水と反応させ硝酸を得る
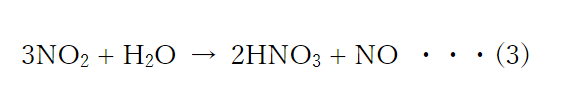
二酸化窒素は水と反応せさせると硝酸になります。
(3)式では副生成物として一酸化窒素が得られますが、この一酸化窒素は回収して再び(2)の反応に使用します。
この反応をまとめると、
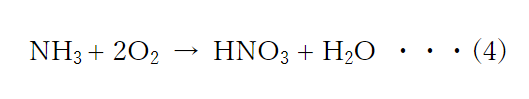
という反応になります。
例題

例題の解答
質量パーセント濃度70%なので、10×0.7=7.0kg=7000gの硝酸を得る必要があります。
この硝酸の物質量は硝酸の分子式63なので、
7000÷63=111mol
式(4)から硝酸1molを得るのに必要なアンモニアは1mol
よって必要なアンモニアの物質量は111molなので、必要なアンモニアの体積は
111×22.4=2.5×103L


コメント