酸化反応・還元反応の4つの定義を解説します。
酸化還元反応の4つの定義
酸化反応・還元反応は以下の4つの観点から考えられます。
- 酸素を受け取っているか?失っているか?
- 水素を受け取っているか?失っているか?
- 電子を受け取っているか?失っているか?
- 酸化数が増加したか?減少したか?
ひとつずつみていきましょう。
酸素を受け取っているか?失っているか?
反応の前後で酸素原子を受け取っているなら酸化、失っているなら還元です。
酸素が増えてるから「酸化」覚えやすいですね。
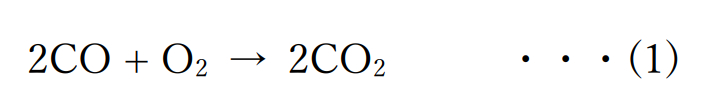
反応の前後で酸素が増えているので、上の化学反応式で一酸化炭素は酸化されているといえます。
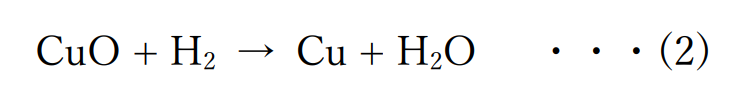
反応の前後で酸素が減っているので、上の化学反応式で酸化銅(Ⅱ)は還元されているといえます。
水素を失っているか、受け取っているか
反応の前後で水素原子を受け取っているなら還元、失っているなら酸化です。
酸素を用いたものと逆になります。
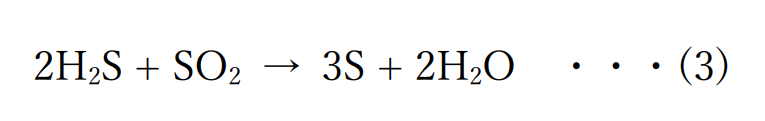
反応の前後で水素を失った硫化水素は酸化されているといえます。
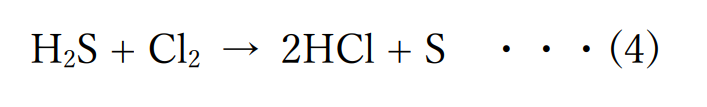
反応の前後で水素を受け取った塩素は還元されているといえます。
電子を受け取っているか?失っているか?
酸化還元を酸素・水素の受け渡しの定義から拡張して、電子の受け渡しでも定義できます。
電子を失っていれば酸化・電子を受け取っていれば還元です。
塩素は電子を受け取っているので酸化されいるといえます。
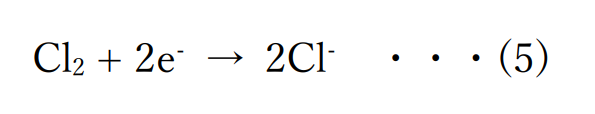
過酸化水素は原子を失っているので、還元されているといえます。
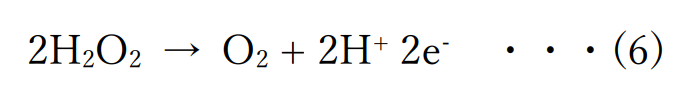
酸化数が増加したか減少したか
酸化されたか還元されたかを統一的に考えるために酸化数という考え方を導入します。
酸化数が増加した場合を酸化、酸化数が減少した場合を還元といいます。
酸化と還元反応
酸素や水素を失う物質があればどこかに受け取る物質があります。
同様に、電子を失う物質があればどこかに受け取る物質があるはずです。
そのため、酸化反応と還元反応は同時に起こるといえます。
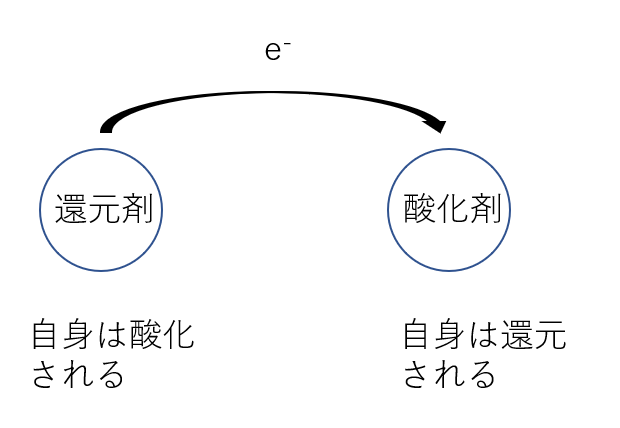
酸化剤と還元剤
相手の物質を酸化させる能力のある物質を酸化剤といいます。
このとき酸化剤は還元剤から電子を受け取り、酸化剤自身は還元されます。
相手の物質を還元させる能力のある物質を還元剤といいます。
このとき還元剤は酸化剤に電子を与え、還元剤自身は酸化されます。


コメント